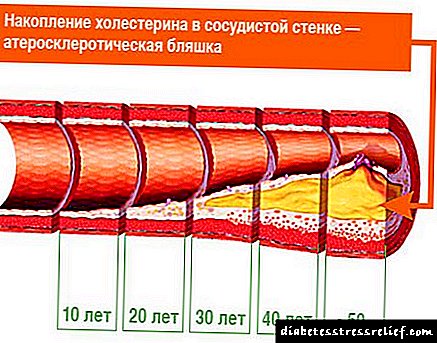
HÆTTUN á fitumyndunarmeðferð og Atherosclerosis: brýnt vandamál og greining
Æðabreytingar í æðum eru einkennandi fyrir næstum alla einstaklinga eldri en 40 ára, munurinn er aðeins á breytingastigi. Þróun æðakölkunar er nátengdur ferli kólesterólflutnings til slagveggs sem hluti af lítilli og mjög lítilli þéttleika fitupróteinum og aðferðum við að fjarlægja kólesteról úr slagvegg með því að nota háþéttni fituprótein. Ef hlutfallinu „lítill og mjög lítill þéttleiki lípíðs / háþéttni fituefna“ er haldið sem 3: 1, kemur æðakölkun ekki fram jafnvel með mikið innihald (meira en 6,21 mmól / l) kólesteról í plasma. Í klínískri framkvæmd er kólesteról stuðullinn af æðakölkun notaður:
þar sem CO er styrkur heildarkólesteróls, SLVP er styrkur háþéttni fitukólesteróls.
Þetta hlutfall er tilvalið hjá nýburum, hjá fólki á aldrinum 20-30 ára, gildi þess er á bilinu 2 til 2,8, eldra en 30 ára (án klínískra einkenna um æðakölkun), það er á bilinu 3,0-3,5 og hjá einstaklingum með kransæðahjartasjúkdóm umfram 4, nær oft 5-6 eða hærri.
Eins og er er talið að aðalatriðið við þróun æðakölkun séu þungamiðjur í uppbyggingu og virkni æðaþelsfrumna í æðum. Allur skaði á æðaþelsinu (verkun eiturefna, ónæmisfléttna, bólgumeðferðarmiðla, kólesteróls, breyttra lípópróteina osfrv.) Eykur gegndræpi þess, leiðir til þess að einfrumur kemast undir endothelium og umbreytingu þeirra í átfrumur.
Á yfirborði átfrumna eru viðtökur fyrir bæði óbreyttar og breyttar lítilli þéttleika fituefna. Þessir viðtakar draga ekki úr virkni við uppsöfnun kólesteróls í átfrumum. Síðarnefndu, sem safnast fituefnum, breytast í froðufrumur (innihalda mikið af estruðu kólesteróli). Endothelium, of mikið af froðufrumum, byrjar að dragast saman og átfrumur koma í snertingu við blóð. Þeir seyta mörg merkjaefni út í umhverfið, þar á meðal þau sem breyta sléttum vöðvafrumum sem hafa viðtaka fyrir vaxtarþætti. Útbreiðsla sléttra vöðvafrumna í miðlaginu og flæði þeirra inn í innra lagið hefst. Uppsöfnun breyttra sléttra vöðvafrumna mettaðar með fitudropum breytast oftast í fjölgandi veggskjöldur.
Breyttar sléttar vöðvafrumur mynda kollagen, elastín og aðra þætti stoðvefur vefjanna í æðakölkun. A trefja veggskjöldur myndast. Í framtíðinni er atheromatous niðurbrot veggskjalda, úrkoma kólesteról kristalla og kalsíumsölt, sem ertir nærliggjandi vef, veldur þrengingu á holrými í skipunum og segamyndun, sem getur leitt til hjartaáfalls og heilablóðfalls, er mögulegt. Á fyrstu stigum æðakölkunar koma fram staðbundnir og altækir efnaskiptasjúkdómar kólesteróls og fitupróteina - dyslipo-proteinemia. Í flestum tilfellum eykst innihald aterógen agna í blóðvökva, sem aðal hluti þess er kólesteról, sem prótein - apóprótein B. Þetta leiðir til staðbundinnar oxunar lágþéttlegrar lípópróteina, uppsöfnun breyttra lípópróteina með lágum þéttleika og myndun æðakölkunarplatna. Með lítinn styrk and-mótefnamyndandi lípópróteina í háum þéttleika í blóði (í 30% tilvika) á sér stað hröðun æðakölkun jafnvel með lágu stigi heildarkólesteróls (minna en 5,18 mmól / l).
Fosfólípíð og fjölómettað fitusýrur hafa and-mótefnavaka eiginleika. Þau takmarka frásog kólesteróls í matvælum í smáþörmum, örva myndun gallsýra í lifur, hindra myndun og seytingu lípópróteina með mjög lágum þéttleika með lifrarfrumum, draga úr styrk lítilli þéttleika fitupróteins í blóðvökva, hindra synthetromboxane A og samloðun blóðflagna og örva nýmyndun prostacycellíns.
Kólesteról, þríglýseríð og mettaðar fitusýrur hafa atherogenic eiginleika. Styrkur aterógen lípópróteina í blóði getur aukist vegna minnkunar á hraða útskilnaðar frá blóði til lifrar, aukningar á tíðni og myndun og brot á umbroti lípópróteina í plasma, þ.mt myndun óeðlilega breyttra lípópróteina.
Truflun á umbroti kólesteróls á sér stað við eftirfarandi skilyrði: í fjarveru lítíþéttni lípóprótein viðtaka á yfirborð frumunnar. Nánar tiltekið: blóðfrumnafæð er ómögulegt, vegna þessa: stig þessara lípópróteina í plasma eykst (arfgeng kólesterólhækkun er tegund II af blóðfitupróteini í blóði) og ósértæk uppsöfnun magnar: frumur reticuloendothelial kerfisins fanga lípóprótein, sem leiðir til óregluaðs uppsöfnunar kólesteróls og estera þess í frumunni,
aukning á skyldleika lípópróteina við himnuna vegna kólesterólmettunar á ytra lagi mjög lítilli þéttleika fitupróteina (tegund III blóðfitupróteinsskortur): bein skaðleg áhrif umfram kólesteróls á æðaþels sléttvöðva í æðum. Á tjónasvæðinu eiga sér stað viðloðandi blóðflögur og losun vaxtarþáttar. Aukning á gegndræpi stuðlar að því að frumur eru teknar af fitupróteinsögnum, tilkoma örskemmda, flæði hvítfrumna úr æðarlaginu inn í skipsvegginn, myndun æðakölkunarplata
streitu, sem flýtir fyrir þróun æðakölkun. Aukning á styrk adrenalíns og angíótensíns í blóði veldur lækkun á æðaþelsfrumum, aukningu á eyðunum á milli þeirra og uppsöfnun mjög lítils og lágþéttnipípópróteina í miðlaginu,
umfram lágþéttni lípóprótein í blóðvökva (magn þeirra í plasma samsvarar útfellingu kólesteróls). Lítilþéttni lípóprótein geta leitt til myndunar rosette-myndandi fléttna, það er örvun á ónæmisferlinu og skemmdum á æðum vegg,
lítið innihald af háþéttni fitupróteinum, sem, í snertingu við yfirborð trefjabólga, æðaþels og sléttar vöðvafrumur, fangar kólesteról. Kólesteról er estert og flutt sem hluti af háþéttni lípópróteinum til lifrarinnar. Þessi lípóprótein keppa um viðtaka með lítinn og mjög lítinn þéttleika fitupróteina og koma í veg fyrir að kólesteról komist í frumur. Þeir geta flutt brott kólesteról í gegnum vatnsfasann í samræmi við þéttni stigsins og þeir skila einnig umfram þríglýseríðum og kólesteróli í gegnum viðtaka í fitu undir húð,
brot á ferlum kólesterólesterunar í háþéttni lípópróteinum og flutningi þess milli einstakra flokka lípópróteina. Þetta dregur úr getu háþéttni lípópróteina til að fjarlægja kólesteról úr vefjum. Hjá sjúklingum með kransæðaæðakölkun eru fitusprótein með mikla þéttleika auðgað í ómótaðu kólesteróli og lípóprótein með lágum þéttleika auðgað í kólesterólesterum,
erfðagalli apólíprópróteina og viðtaka þeirra, lípópróteins og kólesterólumbrotsensíma (arfgengar gerðir af hraðari æðakölkun). Í lifur breytist myndunarhraði og niðurbrot lípópróteina í blóðinu. Mismunandi sameindagallar komu fram í mismunandi fjölskyldum, sem leiddu til ójafnvægis kólesteróls annað hvort í frumum eða í lípópróteinum í blóðrásinni.
Bætt við þann dag: 2015-11-23, Skoðað: 655 | Brot á höfundarrétti
Bókmenntir
1. Libov I. A., Cherkesova S. V., Roitman A. P. Nútíma þættir dyslipoproteinemia og hagnýtar aðferðir við meðferð þeirra // Medical Medical Journal. 3. 1998. S. 34-37.
2. Thompson G. R. Leiðbeiningar um blóðfituhækkun. MSD, 1990.
3. Spector A. V., Vasilyeva E. Yu. Hjartalækningar: lyklar að greiningunni. Vidar, 1996, bls. 295-309.
4. Berk B. C., Weintraub W. S., Alexander R. W. Hækkun C-viðbragðs próteins í „virkri“ kransæðasjúkdómi // Am. J. Cardiol. 1990: 98: 2219-2222.
5. Haverkate F., Thompson S. G., Pyke S. D. M. o.fl., fyrir evrópsku samstilltu aðgerðir vegna segamyndunar og fötlunar Angina Pectoris rannsóknarhóps. Framleiðsla C-hvarfgjarns próteins og hætta á kransæðasjúkdómum í stöðugu og óstöðugu hjartaöng · Lancet. 1997, 349: 462-466.
Vanstarfsemi í endaþarmi
Nútímarannsóknir telja að fyrsta stigið í þróun æðakölkun sé skemmdir á innra yfirborði slagæðarinnar. Það er mikið af gögnum fyrir þessa kenningu:

- Í fyrsta lagi eru fyrstu skellurnar alltaf staðsettar á þeim stöðum þar sem skipsgreinarnar eru grendar. Við aðskilnað aðalskipsins skapast ókyrrðarsvæði, því er hættan á skemmdum á innri húð skipsins á þessum stað alltaf hærri.
- Í öðru lagi hefur það lengi verið vitað að fíkn í tóbak gegnir hlutverki í þróun sjúkdómsins. Og tóbaksreykur hefur neikvæð áhrif á starfsemi æðaþelsfrumna, vegna þess að aukning á magni kolmónoxíðs í blóðinu er tekið fram súrefnisskortur í frumum.
- Í þriðja lagi eykur slagæðarháþrýsting álag á skipin og er einnig þáttur sem eykur hættuna á æðakölkun.
Um kólesteról
Í dag eru fáir sem ekki heyra að hlutverk kólesteróls í þróun æðakölkun væri mjög þýðingarmikið. En það vita ekki allir hvað þetta efni er. Á meðan er þetta einn fulltrúa í flokki steróla, sem gegnir mikilvægu hlutverki við náttúrulega líffræðilega ferla í líkamanum. Helstu hlutverk kólesteróls:
- sköpun gallsýra
- D3 vítamín myndun
- framleiðslu kynhormóna og nýrnahettna.
Það fer eftir mataræði, um það bil 300-500 mg af kólesteróli fer í mannslíkamann daglega. Í vörum getur þetta lípíð verið til staðar í frjálsu eða bundnu ástandi.
En jafnvel í síðara tilvikinu mun klofningur og losun ókeypis kólesteróls eiga sér stað í smáþörmum. Í þörmum frásogast kólesteról, það er notað til efnaskipta og annarra líffræðilegra ferla. 
Dreifing þessa fitu í líkamanum er misjöfn. Mest af öllu kólesteróli er haldið í heilaberki nýrnahettna, heila, taugavef. Síst af öllu eru lípíð í vefjum stoð- og beinvöðva.
Í meginatriðum er nýmyndun kólesteróls hægt að framkvæma í næstum hvaða frumu líkamans. Oftast er þetta efni þó framleitt í lifur og (í miklu minna magni) í smáþörmum. Undir áhrifum ákveðinna þátta eykst kólesterólframleiðsla. Þessir þættir fela í sér:
- geislun
- ójafnvægi í hormónum með fjölgun skjaldkirtilshormóna, insúlín.
Ráðgjöf! En með aukinni framleiðslu á sykurstera (hormónum sem eru framleiddir í nýrnahettum) og hungri dregur úr nýmyndun kólesteróls.
Í ljós kom að steról í blóðvökva er ekki í hreinu ástandi, heldur í formi lípópróteina (fléttu kólesteróls með próteinum). Lipoproteins eru í þremur mismunandi gerðum:
- mjög lítill þéttleiki (heildarmagn þeirra er ekki meira en 10%),
- lítill þéttleiki (þetta er algengasta tegund slíkra lípópróteina í plasma um 65-70%),
- mikill þéttleiki.
Það fer eftir hlutfalli lípópróteintegunda, er hættan á að fá æðakölkun ákvarðað. Fyrir þetta er sérstök greining framkvæmd með ákvörðun á brotum og síðan er stuðullinn reiknaður með því að nota sérstaka formúlu.
Ráðgjöf! Það öruggasta hvað varðar þróun æðakölkun er hlutfall lípópróteintegunda sem sést hefur hjá ungum börnum, stuðull þeirra er eining. Hjá ungu fólki (u.þ.b. 20 ára) er kjörhlutfall vísir frá 2 til 3. Hjá fólki eldri en 30 ætti stuðullinn ekki að fara yfir 3,5 (fyrir hjartasjúkdóma getur hann orðið 6).
Skipta myndun vélbúnaður
Við myndun veggskjöldur eru þrjú stig aðgreind:
- fitusjúkdómur: myndun lípíðblettur eða ræmis á veggjum skips,
- fitukölkun: útliti trefjavefjar,
- myndun flókins veggskjölds, kölkun.
Lípíðblettur er lítil (þvermál ekki meira en 1,5 mm) staðsett á innra yfirborði slagæðar. Froðafrumur eru aðallega samsettar af þessari gulu myndun, þær eru samsettar af T-eitilfrumum og fitu. Að auki eru sléttar vöðvafrumur og átfrumur til staðar í samsetningu myndunarinnar.
Þegar stærð fitublettanna eykst, sameinast þeir, sem leiðir til útbreidds ræmis af sömu samsetningu. Blettir og rönd myndast á þeim stöðum þar sem aðal skemmdir eru á legslímu.
Ráðgjöf! Tilteknu hlutverki í skemmdum á innra yfirborði skipsins og myndun fitublettar er falið óhagstæðum þáttum. Einkum reykingar, klamydísk eða veirusýking, slagæðarháþrýstingur osfrv.
Í sjálfu sér leiðir myndun blettur ekki til skemmda á skipinu. Þar að auki byrja slíkir blettir að myndast í barnæsku. Talið er að við 25 ára aldur geti lípíðmyndanir upptekið allt að helminginn af innra yfirborði ósæðarinnar. Í slagæðum sem fæða heilann birtast slíkir blettir í um það bil 40 ár.
Fituæxli
Annað stig í myndun meinafræðilegrar myndunar (veggskjöldur) er vöxtur trefjavefjar. Á svæðinu við myndaða blettinn (ræmuna) byrja ungar frumur að myndast smám saman, sem leiðir til vaxtar bandvefs.

Þegar það þroskast á sér stað þykknun á veggnum og veggskjöldur myndast - myndun sem rennur út í holrými skipsins. Þetta skapar hindrun fyrir blóðflæði. Á fyrsta stigi myndunar æðakölkunarmyndunar hefur veggskjöldur áberandi fitukjarna.
Í þessu tilfelli er rammi bandvefs þunnur. Þessi myndun er kölluð „gul“, hún hefur lítil áhrif á blóðflæðið. Þar sem hylkin í bandvef er þunn, skemmist það nokkuð auðveldlega.
Á síðari stigum þróunar hefur myndun myndað þéttan ramma bandvef. Það er kallað „hvítur veggskjöldur“ og hefur alvarleg áhrif á blóðskilun (blóðhraði).
Veggmyndun
Þetta stig þróunar sjúkdómsins einkennist af verulegri aukningu á stærð fitukjarna í þegar myndaðri veggskjöldu. Þetta leiðir til eyðileggingar á trefja beinagrind og tilkomu blæðinga.
Þegar ramma veggskjöldsins er eyðilögð á sér stað sáramyndun, sem er aðalástæðan fyrir myndun blóðtappa. Á lokastigi sést uppsöfnun kalsíums í vefjum skellunnar, sem leiðir til þjöppunar og aukningar á stærð skellisins.

Helsta afleiðing myndunar flókinnar æðakölkunarmyndunar er útlit blóðtappa við skipvegginn. Með aðskilnað blóðtappa getur það stíflað skipið, takmarkað blóðflæði verulega.
Ráðgjöf! Það er á þessu stigi þróunar æðakölkun sem sjúklingar upplifa fylgikvilla - þróun heilablóðfalls (með skemmdum á skipum heilans), hjartaáfalli (með þróun æðakölkun í kransæðum) osfrv.
Fylgikvillar
Ofangreint fyrirætlun um myndun veggskjölds gerir okkur kleift að skilja afleiðingar þróunar æðakölkunar. Þetta er:
- hemodynamic breytingar vegna minnkunar á æðum holrými,
- sáramyndun á trefjahylkinu þegar það rofnar, myndun blóðtappa,
- útfelling kalksölt í veggskjölduvef sem eykur þéttleika hans verulega.
Tegundir veggskjöldur
Með æðakölkun geta skellur verið truflanir og ekki. Þessi eign fer eftir lögun, stærð og uppbyggingu. Trefjavef er aðallega í kyrrstöðu veggskjöldur og lípíð ræður ríkjandi í óstöðugum skellum. Static formations vaxa mjög hægt, svo ástand sjúklingsins breytist ekki í mörg ár. Óstöðug veggskjöldur hafa stóran kjarna og þunna trefjahimnu.

Slíkar veggskjöldur rofna auðveldlega og sárast, sem leiðir til blóðtappa. Það er nærvera óstöðugra veggskjalda sem gegnir aðalhlutverki í þróun alvarlegra fylgikvilla æðakölkun.
Svo að meingerð æðakölkun er mjög flókið ferli. Ákveðið hlutverk í þróun sjúkdómsins er ekki aðeins leikið af innri þáttum, heldur einnig af slæmum venjum sjúklingsins. Veitir þróun sjúkdómsfíknar við feitan mat, reykingar, skort á hreyfingu, svo og smitsjúkdóma og truflanir á hormónum í líkamanum. Til að koma í veg fyrir þróun sjúkdómsins er vert að fylgjast reglulega með magni kólesteróls í plasma.